Батарейки различных типов давно и прочно вошли в повседневную жизнь. Они используются во всевозможных электрических устройствах со слабыми токами, в качестве источника питания. Несмотря на внешние существенные отличия, устройство батарейки любого типа имеет общие черты и принципы. Различия могут быть только в составе химических веществ, с помощью которых выделяется электрическая энергия.
Типовое устройство батарейки
Батарейка, изготовленная в заводских условиях, включает в свой состав несколько специальных химических реагентов, которые, взаимодействуя между собой, выделяют энергию – тепловую и электрическую. Кроме того, в каждой батарейке имеются электроды – катод и анод, создающие соответствующие полюса – положительный и отрицательный.
Все реагенты разделяются при помощи специальной прокладки, которая не позволяет их составным частям перемешиваться. Тем не менее, эта прокладка способна пропускать электролит, находящийся внутри батарейки в жидком виде. Между разными твердыми реагентами и жидким электролитом происходят химические реакции, в результате которых образуются положительный и отрицательный заряды. Полюсность заряда напрямую зависит от химического состава того или иного реагента. Прокладка, расположенная между ними, не позволяет нейтрализовать положительный и отрицательный заряд.
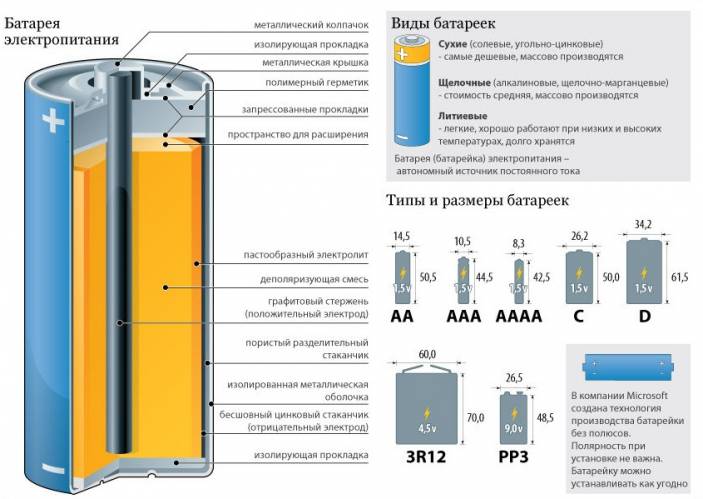
Дополнительные элементы батарейки
Для снятия заряда и вывода его на контакты во внутрь анодного реагента помещается специальный токосниматель в виде штыря. Токосниматель катода расположен под внешней гильзой, являющейся ее оболочкой. И тот и другой токосниматели, оканчиваются электрическими контактами, соответственно анодом и катодом. Работа начинается с химической реакции, затем на реактивах происходит разделение зарядов и их последующий переход на токосниматели. Окончательно заряды поступают на раздельные электроды и, непосредственно, в электронное устройство.
В устройстве щелочных (алкалиновых) батареек применяется цинк в порошкообразной форме. Для того, чтобы замедлить расход цинка, некоторое время назад производились добавки в порошок химических элементов – ртути и кадмия. Поскольку эти добавки оказались вредными, их перестали применять. В современных конструкциях батареек используются более дорогостоящие, но менее вредные вещества, такие как индий, свинец и прочие. В качестве анодного реактива применяется оксид марганца совместно с электролитом, которым в данном случае является щелочь.
Щелочные батарейки могут иногда протекать. Это происходит, когда нарушена герметичность из-за возможных внешних повреждений гильзы, или, когда внутреннее давление становится выше нормы. Солевые батарейки имеют аналогичную конструкцию и более низкую стоимость. Их основное отличие в том, что катодная масса заменяется цинковым корпусом. Угольный токосниматель расположен по центру. Хлорид, используемый как электролит, не что иное, как соль соляной кислоты. Именно она и послужила названием для данного вида батареек.